|
Getting your Trinity Audio player ready...
|
Die Implantologie zählt heute zu den am besten untersuchten Disziplinen der Zahnmedizin – und zugleich zu jenen Bereichen, in denen klinische Entscheidungen in besonderem Maße von Erfahrung, individueller Einschätzung und patientenspezifischen Faktoren geprägt sind. Moderne Bildgebung, digitale Planungsprozesse, neue Biomaterialien sowie weiterentwickelte chirurgische und prothetische Konzepte haben das therapeutische Spektrum in den vergangenen Jahren erheblich erweitert. Mit dieser Vielfalt an Möglichkeiten wächst jedoch auch der Bedarf an strukturierter Orientierung. Leitlinien nehmen in diesem Spannungsfeld eine zentrale Rolle ein. Sie sind weder als Ersatz für klinische Erfahrung noch als starre Handlungsanweisungen zu verstehen. Vielmehr bieten sie einen evidenzbasierten Orientierungsrahmen, der die jeweils verfügbare wissenschaftliche Datenlage mit klinischem Expertenwissen verknüpft – insbesondere dort, wo Langzeitdaten begrenzt sind oder Studienergebnisse heterogen ausfallen. Gerade in komplexen Entscheidungssituationen unterstützen sie eine transparente, nachvollziehbare Risikoabwägung.
Dies gilt in besonderem Maße für die implantologische Versorgung systemisch kompromittierter Patientinnen und Patienten. Systemische Erkrankungen gehören heute zur Regel, nicht zur Ausnahme. Entsprechend verschiebt sich auch der Fokus implantologischer Entscheidungsfindung: Die Frage lautet zunehmend weniger „Darf implantiert werden?“, sondern vielmehr „Unter welchen Voraussetzungen ist das individuelle Risiko vertretbar – und wie lässt sich der Langzeiterfolg möglichst zuverlässig absichern?“.
Die aktuellen S3-Leitlinien zeigen hierbei einen klaren gemeinsamen Trend: weg von pauschalen Kontraindikationen, hin zu einer differenzierten, individualisierten Risikostratifizierung. Die Deutsche Gesellschaft für Implantologie (DGI) verfolgt bei der Erstellung und Aktualisierung ihrer Leitlinien konsequent das Ziel, wissenschaftliche Sorgfalt mit hoher klinischer Relevanz zu verbinden. In den vergangenen Jahren wurden mehrere Leitlinien überarbeitet oder neu gefasst, die sich explizit mit systemischen Risikokonstellationen befassen.
Der vorliegende Übersichtsartikel fasst die wesentlichen Aussagen der aktuell gültigen DGI-Leitlinien zu vier in der Praxis besonders relevanten Konstellationen zusammen: Diabetes mellitus, Immundefizienz, antiresorptive Medikation sowie vorausgegangene Kopf-Hals-Bestrahlung. Ziel ist es, die leitlinienbasierten Empfehlungen einzuordnen und ihre praktische Bedeutung für den klinischen Alltag herauszuarbeiten – als differenzierte Orientierungshilfe sowohl für allgemein zahnärztlich tätige Kolleginnen und Kollegen als auch für implantologisch spezialisierte Behandler.
Implantate bei Diabetes mellitus: evidenzbasierte Entscheidungsfindung bei einem häufigen Risikoprofil
Diabetes mellitus ist mit einer Vielzahl oraler Veränderungen assoziiert, darunter eine erhöhte Anfälligkeit für parodontale Entzündungen, verzögerte Wundheilung und Veränderungen der Knochenstoffwechselprozesse. Vor diesem Hintergrund bestand lange Unsicherheit hinsichtlich der Osseointegration und der Langzeitprognose dentaler Implantate bei betroffenen Patienten. Gleichzeitig wächst der Wunsch vieler Diabetiker nach festsitzendem, implantatgetragenem Zahnersatz. Die ausgewertete Evidenz zeigt, dass das Implantatüberleben bei Patienten mit gut eingestelltem Diabetes mellitus mit dem von stoffwechselgesunden Patienten vergleichbar ist. Auch für die Osseointegration liegen keine Hinweise auf eine grundsätzlich eingeschränkte Einheilung vor, sofern eine adäquate glykämische Kontrolle besteht. Für die Praxis bedeutet das: Diabetes ist nicht per se ein Ausschlusskriterium, sondern verlangt eine strukturierte präoperative Einschätzung [1].
Ein zentrales Ergebnis der Leitlinie ist der Hinweis auf ein erhöhtes Risiko für periimplantäre Entzündungen bei Patienten mit Diabetes mellitus. Besonders relevant ist dabei weniger die Diagnose „Diabetes“ an sich, sondern der Grad der metabolischen Kontrolle. Eine unzureichend eingestellte Hyperglykämie ist mit einer erhöhten Inzidenz periimplantärer Erkrankungen assoziiert. Damit rückt die Entzündungsprävention (parodontal wie periimplantär) in den Vordergrund. Die Leitlinie betont, dass vor einer Implantation eine stabile Stoffwechsellage angestrebt werden sollte. HbA1c-Werte dienen hierbei als praxisrelevanter Orientierungsparameter. Eine gute interdisziplinäre Zusammenarbeit mit Hausärzten oder Diabetologen wird ausdrücklich empfohlen – insbesondere dann, wenn zusätzliche Risikofaktoren (Rauchen, Parodontitis, Adipositas, kardiovaskuläre Begleiterkrankungen) hinzukommen [1].
Auch augmentative Maßnahmen können bei Patienten mit Diabetes mellitus durchgeführt werden. Die verfügbare Evidenz zeigt keine grundsätzlich erhöhte Komplikationsrate bei gut eingestellten Patienten. Entscheidend sind eine sorgfältige Indikationsstellung, ein atraumatisches chirurgisches Vorgehen sowie ein konsequentes perioperatives Management – und vor allem die Sicherstellung einer entzündungsfreien Ausgangssituation [1].
Für die tägliche Praxis bedeutet dies: Diabetes mellitus stellt keine generelle Kontraindikation für eine Implantatversorgung dar. Vielmehr ist eine individuelle Risikoanalyse erforderlich, die den Stoffwechselstatus, Begleiterkrankungen, parodontale Situation und die Fähigkeit zur langfristigen Nachsorge berücksichtigt. Eine strukturierte Aufklärung über mögliche Risiken sowie ein engmaschiges Recall- und Prophylaxekonzept sind essenziell. Implantattherapien bei Patienten mit Diabetes mellitus sind also bei guter glykämischer Kontrolle sicher und prognostisch vertretbar. Entscheidend ist nicht die Diagnose allein, sondern die individuelle Stoffwechsellage und das konsequente periimplantäre Langzeitmanagement [1].
Implantate bei Patienten mit Immundefizienz: differenzierte Risikobewertung statt genereller Kontraindikation
Systemische Immundefizienzen stellen aufgrund ihrer Heterogenität eine besondere Herausforderung in der implantologischen Therapieplanung dar. Während früher häufig Zurückhaltung gegenüber implantologischen Maßnahmen bestand, zeigen aktuelle evidenzbasierte Empfehlungen, dass auch bei immundefizienten oder immunsupprimierten Patienten eine Implantatversorgung unter definierten Voraussetzungen möglich ist. Die S3-Leitlinie „Dentale Implantate bei Patienten mit Immundefizienz“ differenziert klar zwischen unterschiedlichen Ursachen und Ausprägungen der Immunsuppression.
Unter dem Begriff der Immundefizienz werden sowohl primäre angeborene Störungen als auch sekundäre Formen zusammengefasst. Zu Letzteren zählen unter anderem HIV-Infektionen, immunsuppressive Therapien im Rahmen von Autoimmunerkrankungen, Chemotherapien sowie die medikamentöse Immunsuppression nach Organtransplantationen. Für die implantologische Entscheidungsfindung sind daher weniger die Diagnose an sich, sondern vielmehr der klinische Status, die Krankheitsaktivität und die begleitende Medikation ausschlaggebend [2].
Die Leitlinie kommt zu dem Ergebnis, dass bei den meisten immundefizienten Patienten keine signifikant erhöhte Implantatverlustrate im Vergleich zu gesunden Kontrollkollektiven nachweisbar ist, sofern sich die Grunderkrankung in einer stabilen oder inaktiven Phase befindet. Insbesondere bei HIV-positiven Patienten zeigen die vorliegenden Daten unter stabilen Bedingungen vergleichbare Implantatüberlebensraten [2].
Auch bei Patienten nach Organtransplantation konnte unter laufender immunsuppressiver Medikation kein konsistenter negativer Einfluss auf die Osseointegration festgestellt werden. Die Evidenz basiert hier überwiegend auf Kohortenstudien und Fallserien, weist jedoch insgesamt keine Hinweise auf eine generelle Kontraindikation auf. Ein differenzierter Blick ist bei be-stimmten Erkrankungen erforderlich. Für Patienten mit Morbus Crohn existieren Hinweise auf ein erhöhtes Risiko für frühe Implantatverluste. Die Leitlinie empfiehlt daher ausdrücklich, diese Patienten über eine potenziell eingeschränkte Implantatprognose aufzuklären. Ursache könnten immunvermittelte Prozesse im Bereich des Knochen-Implantat-Kontakts sowie begleitende Mangelernährungszustände sein. Bei Patienten unter Chemotherapie zeigt die aktuelle Datenlage hingegen keine signifikant erhöhte Implantatverlustrate, sofern die Implantation zeitlich außerhalb intensiver Therapiephasen erfolgt. Eine enge Abstimmung mit den behandelnden Onkologen ist hierbei essenziell [2].
Ein zentrales Thema bei immundefizienten Patienten ist das perioperative Infektionsrisiko. Die Leitlinie betont die Bedeutung einer individuellen Risikoabschätzung, einer konsequenten Sanierung potenzieller Infektionsherde vor Implantation sowie – je nach Risikoprofil – einer perioperativen antibiotischen Prophylaxe. Augmentative Maßnahmen sollten bei immunsupprimierten Patienten besonders kritisch geprüft werden, da Knochenumbau- und Regenerationsprozesse systemisch beeinträchtigt sein können. Eine verlängerte Einheilzeit sowie eine zurückhaltende Indikationsstellung für Sofort- oder Frühbelastung werden empfohlen [2].
Für die prothetische Umsetzung gelten grundsätzlich dieselben funktionellen Kriterien wie bei gesunden Patienten. Die Leitlinie rät jedoch zu hygienefähigen, übersichtlichen prothetischen Konzepten, um das Risiko periimplantärer Entzündungen zu minimieren. Eine strukturierte, risikoadaptierte Nachsorge wird als essenzieller Bestandteil des Behandlungserfolgs hervorgehoben.
Auch bei Patienten mit Immundefizienz gilt: Implantate sind kein grundsätzliches Tabu. Entscheidend ist eine sorgfältige individuelle Risikoanalyse unter Berücksichtigung der Grunderkrankung, der Medikation, der Mundhygienefähigkeit und der langfristigen Nachsorge. Der interdisziplinäre Austausch mit den behandelnden Ärzten spielt dabei eine zentrale Rolle.
Die aktuelle S3-Leitlinie unterstreicht, dass eine implantologische Versorgung bei immundefizienten Patienten bei stabiler Grunderkrankung und angepasstem Therapiemanagement möglich ist. Statt pauschaler Ablehnung ist eine differenzierte, evidenzbasierte Entscheidungsfindung erforderlich, die sowohl medizinische Risiken als auch den potenziellen Gewinn an Lebensqualität berücksichtigt [2].
Implantate bei Patienten unter antiresorptiver Medikation: zwischen Osteonekroserisiko und funktionellem Gewinn
 Spliker, Schiegnitz
Spliker, SchiegnitzDie medikamentöse Behandlung mit Knochenantiresorptiva stellt eine der größten Herausforderungen in der implantologischen Therapieplanung dar. Insbesondere die medikamentenassoziierte Osteonekrose der Kiefer (MRONJ) hat zu einer historisch sehr restriktiven Indikationsstellung geführt. Die S3-Leitlinie „Zahnimplantate bei medikamentöser Behandlung mit Knochenantiresorptiva“ liefert eine differenzierte Grundlage für die klinische Entscheidungsfindung. Knochenantiresorptiva wie Bisphosphonate oder Denosumab werden sowohl bei benignen Erkrankungen (z.B. Osteoporose) als auch bei malignen Grunderkrankungen mit ossärer Beteiligung eingesetzt. Das individuelle Risiko für eine MRONJ wird beeinflusst von Grunderkrankung, Medikament, Applikationsfrequenz und -dauer sowie Begleiterkrankungen, weiterer Medikation und anderen Faktoren. Ein Kernelement der Leitlinie ist die Forderung, bei allen Patienten unter bzw. nach antiresorptiver Therapie vor einer Implantation zunächst das individuelle Osteonekroserisiko zu evaluieren, weil eine Osteonekrose auch Folge einer entzündlichen Implantatkomplikation sein kann. Wichtige Einflussfaktoren sind unter anderem: Grunderkrankung, Applikationsart, Dauer und Frequenz der Medikation, zusätzliche Therapien (z.B. Immun-/Antikörpertherapien, Chemotherapie, antiangiogenetische Therapie, Kopf-Hals-Strahlentherapie) sowie eine vorausgegangene Osteonekrose [3]. Hierzu hat die DGI einen Laufzettel entwickelt, der die Einschätzung übersichtlich macht und das Risiko einer Kiefernekrose in gering/mittel/hoch einstuft (Abb.1).
Notwendige zahnärztliche Eingriffe zur Sanierung von Infekten und zur Reduktion des Infektrisikos sollen vor Implantationen durchgeführt werden; der Heilungsverlauf soll in die Risikoevaluation einfließen. Klinische und radiologische Befunde, die Hinweise auf eine Kompromittierung der Weichgewebeheilung, des Knochenumbaus oder der Knochenneubildungsrate geben, sollen erhoben und in die Entscheidung einbezogen werden. In diesem Kontext betont die Leitlinie, dass chronische oder akute Infektionen, Prothesendruckstellen und weitere lokale Trigger möglichst vorab beseitigt werden sollten. Die Bestimmung des CTX ( -CTX) sollte zur weitergehenden Beurteilung der Knochenresorption und der pharmakologischen Wirksamkeit nicht erfolgen; die klinische Relevanz ist wissenschaftlich nicht erwiesen [3].
Die Motivierbarkeit und Realisierbarkeit einer guten Mundhygiene und periimplantären Hygiene sollte – wegen des möglichen Schweregrades einer entzündlichen Implantatkomplikation – in die Entscheidungsfindung einbezogen werden. Ein wichtiger, praxisnaher Punkt: Implantate können durch Reduktion der Schleimhautbelastung zur Vermeidung von Prothesendruckstellen beitragen und damit das individuelle Osteonekroserisiko senken. Die Implantatindikation soll daher auch dahingehend überprüft werden, ob Prothesendruckstellen vermieden werden können [3].
Bei Patienten mit antiresorptiver Therapie sollten Kieferaugmentationen vermieden oder einer besonders strengen Indikationsprüfung unterzogen werden, da sie erhöhte Anforderungen an vaskuläre Erschließung, Resorption und Knochenneubildung stellen – Prozesse, die unter Antiresorptiva vermindert sein können [3].Die Leitlinie stellt heraus, dass sich die kurzfristige Implantatprognose häufig nicht relevant von Kollektiven ohne Antiresorptiva unterscheidet – weist aber zugleich auf einzelne gravierende Komplikationen (u.a. Osteonekrosen) hin (Abb. 2).
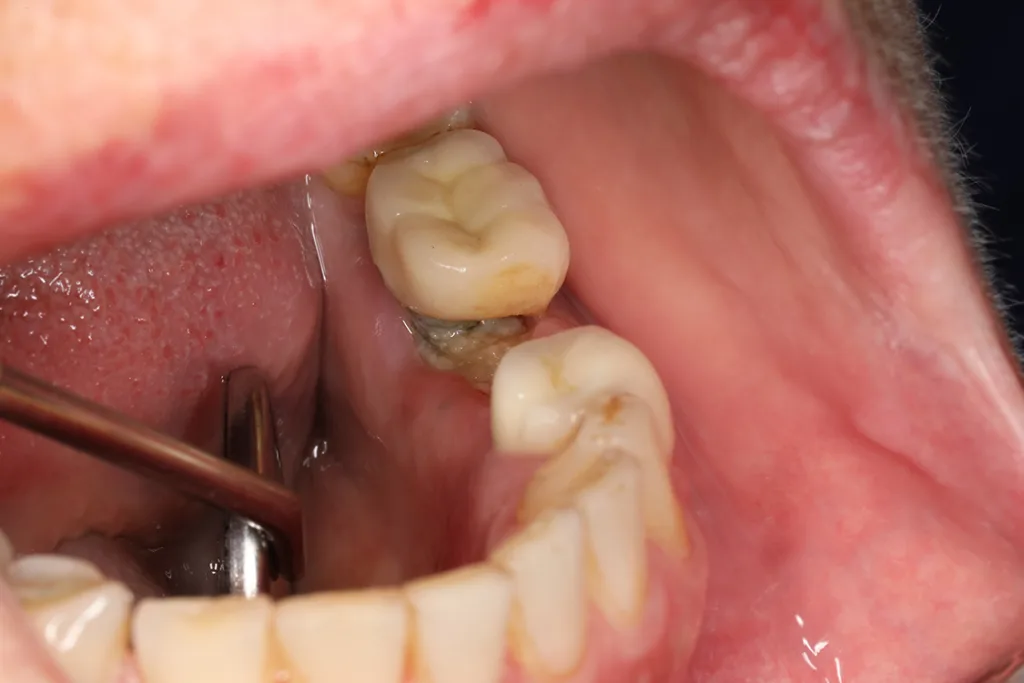 Spliker, Schiegnitz
Spliker, SchiegnitzDer Patient soll vor einer geplanten Implantation über das individuelle Osteonekroserisiko und die dringliche Empfehlung zur strukturierten Nachsorge (inkl. Hinweis auf mögliche Folgekosten) informiert werden. Für einen „Drug holiday“ (zeitweiliges Absetzen) gibt es keine belastbaren Daten; daraus lässt sich keine generelle Empfehlung ableiten. Demgegenüber wird eine perioperative systemische Antibiotikaprophylaxe klar empfohlen. Da Knochenumbau- und Neubildungsrate verringert sein können, kann eine verlängerte Einheilzeit bis zur Belastung sinnvoll sein. Prothetisch wird als Ziel die Reduktion der tegumentalen Belastung formuliert; wo möglich kann ein rein implantatgetragener Zahnersatz helfen, Prothesendruckstellen als Trigger auszuschalten. Außerdem gilt: Patienten sollen in eine risikoadaptierte Nachsorge aufgenommen werden; bei periimplantären Infektionen soll frühzeitig behandelt werden [3].
Implantate sind auch unter bzw. nach antiresorptiver Therapie nicht grundsätzlich kontraindiziert. Zentral sind Risikostratifizierung (insbesondere nach Grunderkrankung und Applikationsform), strikte Infektkontrolle, zurückhaltende Augmentationsstrategie, antibiotische Abschirmung und enges Recall [3]. Auch hierzu gibt es einen Laufzettel, mit Hilfe dessen das Risiko bei antiresorptiver Therapie vor Implantation eingestuft werden kann (Abb. 3).
 Spliker, Schiegnitz
Spliker, SchiegnitzImplantate bei Patienten nach Kopf-Hals-Bestrahlung: hohe Anforderungen an Planung, Risikoabwägung und Nachsorge
Patienten mit vorausgegangener oder geplanter Kopf-Hals-Bestrahlung zählen zu den anspruchsvollsten Kollektiven in der implantologischen Rehabilitation. Neben funktionellen Einschränkungen stehen insbesondere strahlenbedingte Veränderungen von Knochen, Schleimhaut und Speichelfluss sowie das Risiko einer infizierten Osteoradionekrose (IORN) im Fokus. Die aktuelle S3-Leitlinie „Implantat-Versorgung zur oralen Rehabilitation im Zusammenhang mit Kopf-Hals-Bestrahlung“ bietet hierfür eine umfassende Grundlage.
Die Leitlinie differenziert zwischen frühen, meist reversiblen Folgen (z.B. Mukositis) und späten, oft irreversiblen Folgen (Radioxerostomie, Strahlenkaries, Strahlenfibrose, Risiko der IORN). Das Zusammenspiel dieser Faktoren führt häufig zu einer deutlichen Einschränkung der mundgesundheitsbezogenen Lebensqualität – und erklärt, warum implantatgetragene Konzepte für viele Betroffene funktionell und psychosozial relevant sind. Patienten mit Tumor im Kopf-Hals-Bereich sollen vor Beginn der onkologischen Therapie eine Untersuchung, Dokumentation und ggf. Behandlung des Zahnstatus erhalten.
Für Planung und Durchführung chirurgischer Maßnahmen soll eine enge interdisziplinäre Absprache mit Radioonkologen sowie (je nach Setting) Hausarzt/Onkologen erfolgen [4].
Praktisch wichtig: Für eine individuelle Risikozuordnung wird u.a. eine genaue Kenntnis von Verfahren, Dosis, Zielvolumen (inkl. Dosisverteilung in Ober-/Unterkiefer) sowie Begleittherapien (Chemotherapie, „Bone modifiers“ wie Bisphosphonate/Denosumab) als entscheidungsrelevant beschrieben. Eine Abstimmung zwischen implantologisch chirurgischer und prothetischer Planung sollte unter besonderer Berücksichtigung onkologischer Aspekte erfolgen.
Ein zentrales Leitlinien-Statement ordnet die Implantatposition nach knöchernem Lager in eine Risikogradierung ein (von günstig nach ungünstig): unbestrahlter ortständiger Knochen < bestrahlter ortständiger Knochen außerhalb des Zielvolumens < unbestrahlter augmentierter Knochen < bestrahlter ortständiger Knochen innerhalb des Zielvolumens < bestrahlter augmentierter Knochen [4].
Konsequenz: Die prothetisch ideale Implantatposition soll gegen eine chirurgisch risikoärmere oder prognostisch günstigere Position abgewogen werden – ggf. mit bewusster Aufgabe der prothetischen Idealposition zugunsten der chirurgischen.
Nach Kenntnis der Leitliniengruppe liegen praktisch ausschließlich Daten zu Titanimplantaten vor; keramische Implantate sind wissenschaftlich nicht untersucht. Für Implantatdimensionen ergeben sich keine grundlegend anderen Kriterien als ohne Bestrahlung, wobei dicke Weichgewebeschichten nach Rekonstruktionen zu berücksichtigen sind. Zudem lässt sich keine belastbare wertende Empfehlung für submuköse vs. transmuköse Einheilung oder bestimmte Implantatdesigns ableiten. Zusätzlich weist die Leitlinie auf dosimetrische Effekte hin: Metallische Restaurationen können lokal zu Dosiserhöhungen führen; Titanimplantate im Zielvolumen verursachen ebenfalls eine Dosiserhöhung, für die keine gezielten Minderungsmaßnahmen zur Verfügung stehen [4].
Die IORN wird als eine der schwersten lokalen Komplikationen beschrieben; auch bei moderner IMRT sind relevante ORN-Raten im Langzeitverlauf möglich, weshalb eine langfristige klinische Nachkontrolle dringend indiziert ist. Für implantologisch versorgte Patienten ist das entscheidende Ziel: Entzündungen (periimplantär wie dental) früh erkennen und konsequent behandeln, weil infektiöse Trigger eine zentrale Rolle spielen [4].
Implantatgetragene Rehabilitation nach Kopf-Hals-Bestrahlung ist möglich – jedoch klar risikoadaptiert. Die Prognose hängt wesentlich von Lager (ortsständig vs. augmentiert; bestrahlt im Zielvolumen vs. außerhalb), Gesamttherapiesetting und Nachsorge ab. Interdisziplinäre Abstimmung und ein kompromissloses Entzündungsmanagement sind hier Voraussetzung [4].
Gemeinsame Prinzipien aus vier Leitlinien – und was sie für die Praxis bedeuten
Leitlinienübergreifend zeigt sich: Systemische Kompromittierung bedeutet nicht automatisch „nicht implantieren“, sondern lediglich anders planen. In allen vier Themenfeldern sind drei Erfolgsfaktoren wiederkehrend:
- Stabiler Systemstatus (Metabolik/Erkrankungsaktivität/Therapiephase)
- Entzündungsfreiheit vor Implantation und im Verlauf
- Recall-Fähigkeit (Patientenführung, Hygiene, regelmäßige Kontrollen)
Ob periimplantäre Entzündung bei Diabetes, infektgetriggerte Komplikationen bei Immundefizienz, MRONJ bei Antiresorptiva oder IORN nach Bestrahlung: Entzündung ist der gemeinsame Nenner, der aus einem „Risiko“ ein „Problem“ macht. Das unterstreicht den Stellenwert der präoperativen Sanierung und des langfristigen professionellen Erhaltungsprogramms. Bei bestrahlten Patienten ist es explizit formuliert (Abwägung prothetisch ideal vs. chirurgisch prognostisch günstig), gilt aber in allen Modulen: Hygienefähige Prothetik, entzündungsarme Designs und realistische Belastungsstrategien sind Teil der Risikoreduktion. Mit zunehmendem Systemrisiko wird Interdisziplinarität grundlegend immer weniger optional. Diabetes (Hausarzt/Diabetologie), Immundefizienz (Behandler der Grunderkrankung), Antiresorptiva (Onkologie/Orthopädie/Internistik), Bestrahlung (Radioonkologie) – in jedem Modul ist die medizinische Kontextinformation entscheidend, um Zeitpunkt, Risiko und Alternativen korrekt einzuordnen. Je höher das Risiko, desto wichtiger ist eine strukturierte, transparente Aufklärung hinsichtlich Behandlungsnutzen (Funktion, Lebensqualität, Vermeidung von Druckstellen) und Komplikationsmöglichkeiten (Periimplantitis, MRONJ, IORN). Dazu gehört auch die klare Kommunikation, dass Nachsorge und Recall fester Bestandteil der Therapie sind. Generell gilt: Leitlinien ersetzen nicht die klinische Erfahrung, sie strukturieren sie. Gerade bei systemisch kompromittierten Patienten sind sie damit ein unverzichtbares Instrument für eine sichere, verantwortungsvolle Implantologie.
 Entdecke CME Artikel
Entdecke CME Artikel  Entdecke Artikel mit Download
Entdecke Artikel mit Download 





 Mit Google einloggen
Mit Google einloggen
 Mit Facebook einloggen
Mit Facebook einloggen
Keine Kommentare.