|
Getting your Trinity Audio player ready...
|
In Deutschland zeigen 95,1% der jungen Erwachsenen (35- bis 44-Jährige) Anzeichen einer Parodontitis, wobei etwa 18% schwere Verlaufsformen (Stadium III und IV) aufweisen [7]. Die Parodontitis im Allgemeinen ist also eine hochprävalente Erkrankung, bei der eine chronisch-entzündliche Destruktion des Zahnhalteapparates durch das Zusammenspiel von bakteriellen, genetischen und erworbenen Risikofaktoren beeinflusst wird. Genetische Prädisposition bedeutet in diesem Zusammenhang, dass eine Person eine konstitutionelle Anfälligkeit für die Entwicklung einer Parodontitis hat, die sich erst in Verbindung mit anderen pathogenen Faktoren manifestiert [13]. Nicht alle Personen, die die genetischen Risikofaktoren in sich tragen, entwickeln somit die Krankheit im gleichen Ausmaß.
Wenn Parodontitis auf ein seltenes Syndrom hinweist
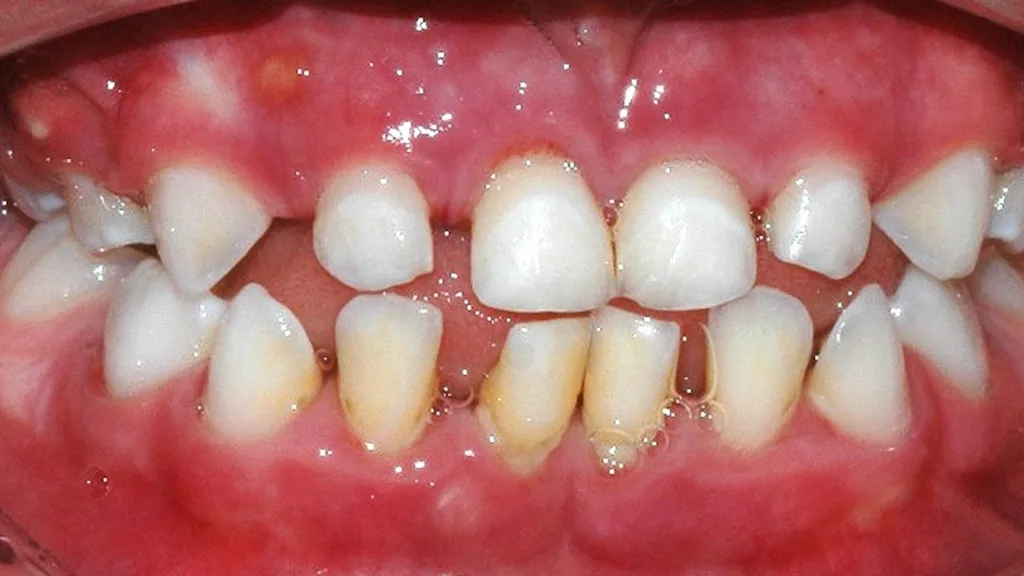
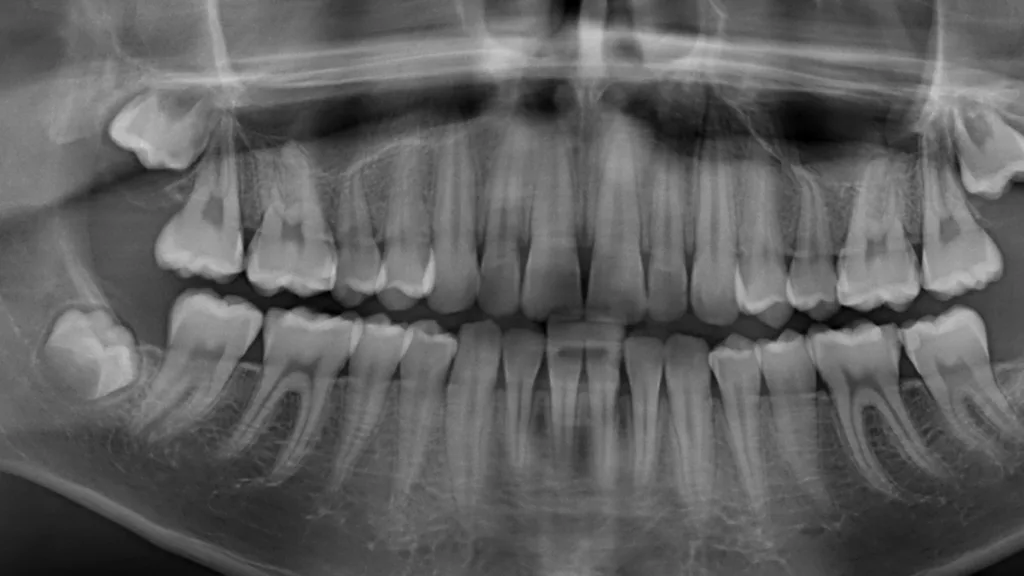
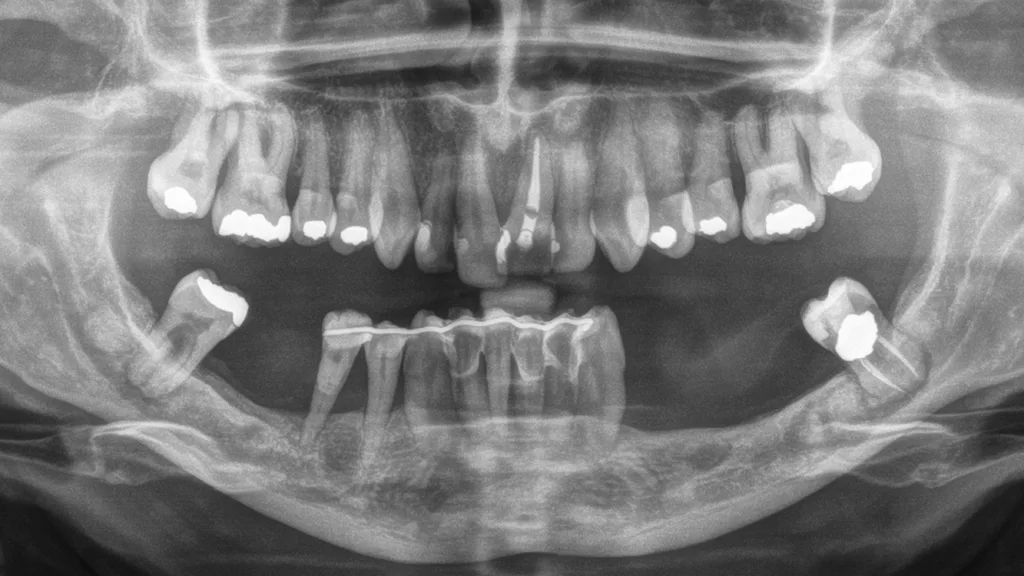
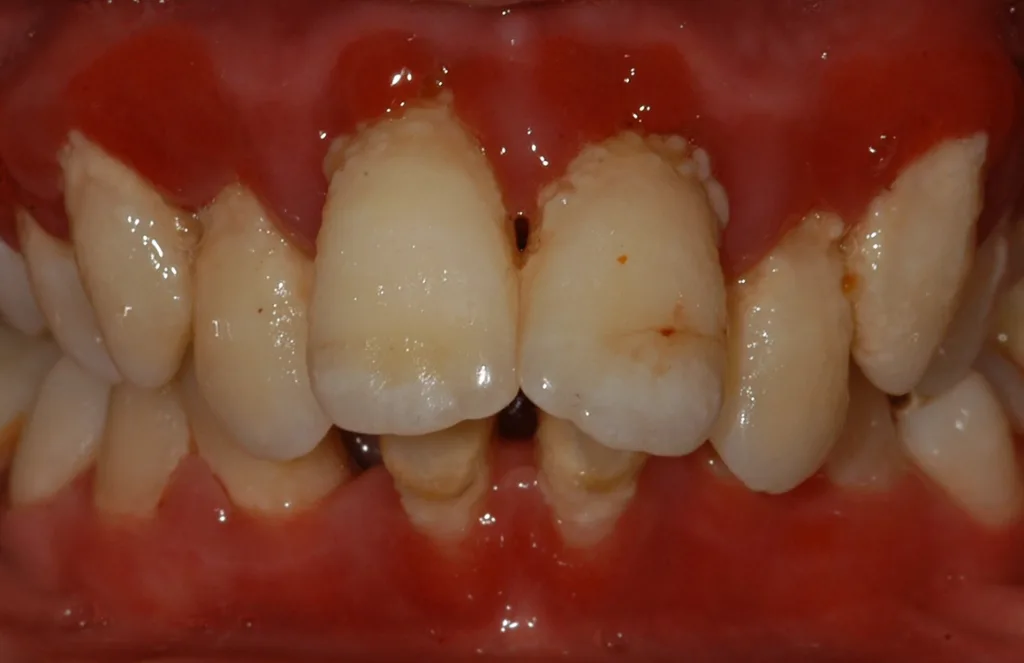
Im Gegensatz dazu existieren eine Reihe seltener Syndrome, bei denen betroffene Personen unabhängig von klassischen Risikofaktoren eine schwere parodontale Destruktion entwickeln. Seltene Syndrome sind (meist) genetisch bedingte Erkrankungen, die durch eine charakteristische Kombination klinischer Symptome gekennzeichnet sind und gemäß europäischer Definition eine Prävalenz von weniger als 1 pro 2.000 Personen aufweisen. In der Parodontologie ist eines der bekanntesten Beispiele das autosomal-rezessiv vererbte Papillon-Lefèvre-Syndrom, das durch eine rasch-progrediente Parodontitis im Kindesalter sowie durch palmoplantare Hyperkeratosen der Hände und Füße gekennzeichnet ist; ursächlich sind Mutationen im Cathepsin-C-(CTSC-)Gen (Abb. 1, Abb. 2).
In der aktuellen Klassifikation der parodontalen und periimplantären Erkrankungen und Zustände werden diese Formen der Parodontitis unter der Kategorie „Parodontitis als Manifestation einer systemischen Erkrankung“ eingeordnet [3]. Ein charakteristisches Merkmal ist die hohe Genotyp-Phänotyp-Korrelation, das bedeutet, dass ein sehr hoher Prozentsatz der von dem Syndrom betroffenen Personen bereits im Kindes- oder Jugendalter eine Parodontitis entwickelt, unabhängig von klassischen Risikofaktoren wie Plaque, Rauchen, Stress oder systemischen Begleiterkrankungen wie Diabetes mellitus. Diese enge Verbindung zwischen genetischem Hintergrund und parodontalem Befund unterstreicht die Bedeutung einer frühzeitigen zahnärztlichen Diagnose und eines spezialisierten Managements bei den Betroffenen.
Seltene, mit Parodontitis assoziierte Syndromerkrankungen
Seltene Syndromerkrankungen, die mit Parodontitis assoziiert sind, können pathogenetisch in drei Hauptgruppen eingeteilt werden: primäre Immundefizienzen, Syndrome mit Haut- oder Bindegewebsbeteiligung sowie Stoffwechsel- und Enzymdefekte.
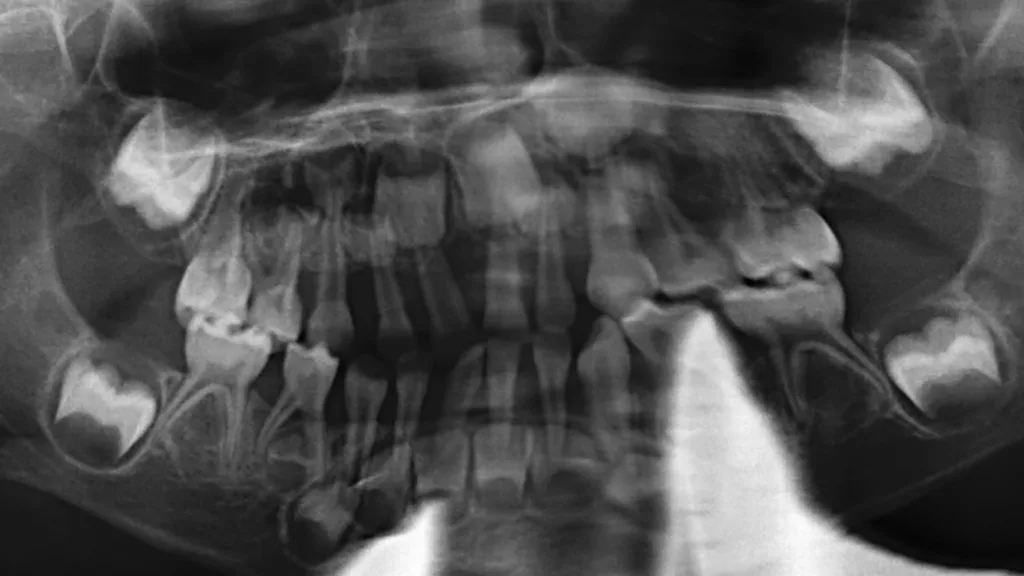
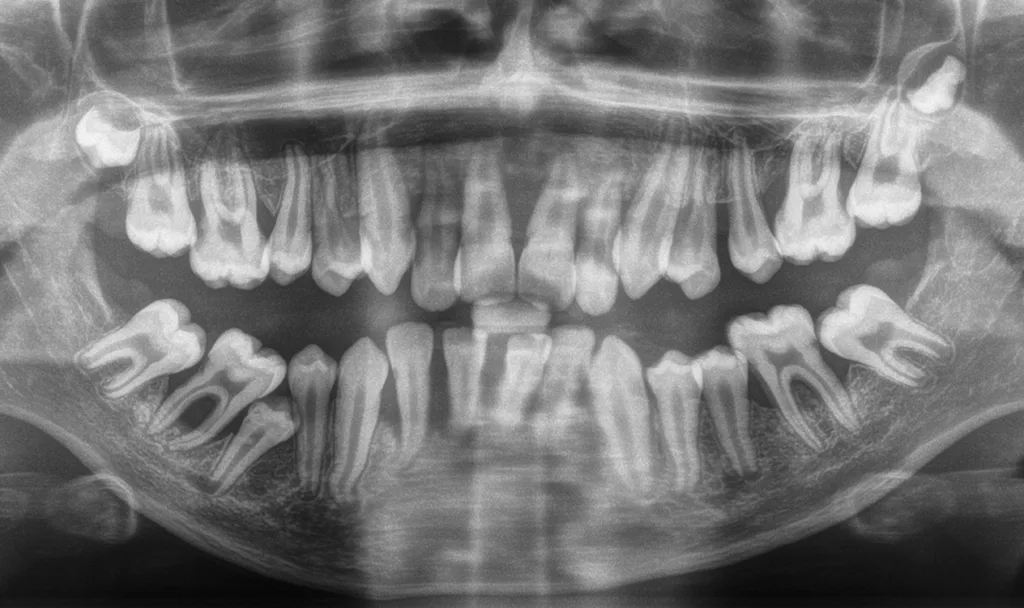
Primäre Immundefizienzen bilden die größte Gruppe an Syndromen, die sich mit einer Parodontitis manifestieren. Diese genetisch heterogenen Erkrankungen beeinträchtigen die Struktur, Reifung, Differenzierung oder Funktion von Organen und Zellen des Immunsystems. Sie werden typischerweise durch pathogene Veränderungen einzelner Gene – sogenannte monogene Mutationen – verursacht. Innerhalb dieser Gruppe sind insbesondere angeborene Störungen in Zahl und Funktion neutrophiler Granulozyten mit Parodontitis assoziiert. Typische Beispiele hierfür sind schwere kongenitale Neutropenien (Abb. 3, Abb. 4) und das Papillon-Lefèvre-Syndrom. Andere Syndrome, wie das Hermansky-Pudlak-Syndrom oder das Chediak-Higashi-Syndrom, resultieren aus Funktionsstörungen lysosomenassoziierter Organellen, die für die normale Aktivität zahlreicher Immunzellen essenziell sind, während wieder andere, wie die Leukozytenadhäsionsdefizienzen, durch eine defekte Leukozytenmigration bedingt sind. Im oralen Bereich führen primäre Immundefizienzen häufig zu rezidivierenden aphthösen Stomatitiden, rekurrentem Herpes, oropharyngealer Candidiasis, Ulzerationen und bakteriellen Infektionen. Diese Infektionen können wiederum eine früh einsetzende und rasch fortschreitende Gingivitis und in der Folge Parodontitis begünstigen.
Syndrome mit Stoffwechsel- oder Enzymdefekten seien als zweite Gruppe genannt, die in der Pathogenese jedoch häufig eine Überlappung mit den Immundefizienzen aufweisen. Ein Beispiel ist die Glykogenose Typ 1b, eine autosomal-rezessiv vererbte Stoffwechselerkrankung, die durch einen Defekt des Glukose-6-Transporters verursacht wird. Dieser beeinträchtigt den Energiestoffwechsel der Neutrophilen, was sowohl deren Zahl verringert als auch ihre Funktion schwächt.
Syndrome mit Haut- oder Bindegewebsbeteiligung, die das epitheliale oder bindegewebige Attachment des Parodonts beeinträchtigen, bilden die dritte Gruppe von Syndromen, die durch eine Parodontitis im Kindes- und Jugendalter gekennzeichnet sind. Eines der wenigen Beispiele hierfür ist das Kindler-Syndrom, eine seltene, autosomal-rezessive Form der Epidermolysis bullosa. Durch Mutationen im FERMT1-Gen, das für das Protein Kindlin-1 kodiert, wird die Bildung von Keratinozyten-Adhäsionsproteinen beeinträchtigt, wodurch die Zelladhäsion sowie die Haut- und Schleimhautintegrität gestört werden. Gleichzeitig ist die Anbindung des Zytoskeletts an die Zellmembran vermindert, was insbesondere in der Gingiva eine erhöhte Gewebefragilität und parodontale Entzündungsprozesse begünstigt.
Abgrenzung der Gruppe
Die Abgrenzung der Kategorien „Parodontitis als Manifestation einer Systemerkrankung“ zu den „Systemerkrankungen oder Zuständen mit Auswirkungen auf das Parodont“ ist nicht immer eindeutig [3], aber definitiv klinisch relevant. Während eine Parodontitis eine entzündliche parodontale Destruktion darstellt und auch als solche therapiert werden muss, können neoplastische Proliferationen unterschiedlicher Zelltypen durch Zerstörung der parodontalen Gewebe eine lokalisierte Parodontitis zwar imitieren, werden aber auf eine antiinfektiöse Therapie nicht ansprechen. Als Beispiel sei die Langerhans-Zell-Histiozytose genannt, eine gutartige, aber lokal zerstörerische Entität, bei der es sich um eine echte neoplastische Proliferation unreifer myeloider dendritischer Zellen aus dem Knochenmark handelt. Aus radiologischer Sicht wurde eine Ähnlichkeit der Knochenläsionen mit einem breiten Spektrum von Krankheiten beschrieben, wie z.B. odontogenen Zysten, bestimmten gutartigen und bösartigen Tumoren, periapikalen Läsionen und eben auch parodontalem Knochenverlust [6]. Somit ist insbesondere bei Erwachsenen die Diagnosestellung erschwert, da sich die Erkrankung in dieser Patientengruppe meist unifokal und ohne weitere klinische Begleitzeichen präsentiert. Im Kindesalter verläuft sie hingegen häufiger multifokal oder multisystemisch.
Syndrome, die primär zahnärztlich diagnostiziert werden müssen
Jede parodontale Destruktion im Kindesalter ist ein alarmierendes Zeichen für eine mögliche syndromale Erkrankung. Der Großteil der seltenen Erkrankungen, die zu einer Parodontitis im Kindes- und Jugendalter führen, wird aufgrund der systemischen Manifestationen bereits im Säuglingsalter durch Pädiaterinnen und Pädiater diagnostiziert. Das bedeutet für Zahnärztinnen und Zahnärzte, dass das betroffene Kind bereits mit der systemischen Diagnose vorstellig wird. Wichtig ist in diesen Fällen das regelmäßige parodontale Screening und striktes Biofilmmanagement von frühester Kindheit an. Nur ein kleiner Teil der genetischen Syndrome, die sich mit einer Parodontitis manifestieren, muss primär zahnärztlich diagnostiziert werden, da die parodontale Destruktion das Hauptmerkmal darstellt. Dazu zählen das Papillon-Lefèvre-Syndrom, die Plasminogendefizienz, das parodontale Ehlers-Danlos-Syndrom, die Odonto-Hypophosphatasie und unter Umständen auch die zyklische Neutropenie.
Das Papillon-Lefèvre-Syndrom (PLS) ist, wenn alle Symptome ausgeprägt sind, durch die generalisierte Parodontitis im Milchgebiss in Kombination mit palmoplantaren Hyperkeratosen klinisch leicht zu diagnostizieren [12]. Allerdings gibt es auch Fälle, in denen nur die Hautveränderungen oder die Parodontitis auftreten. Durch die autosomal-rezessive Vererbung tritt PLS nur auf, wenn beide Allele – das mütterlich und das väterlich vererbte Allel – eines Gens defekt sind. Das können homozygote Mutationen sein, also zwei idente Mutationen, wenn die Eltern einen Verwandtschaftsgrad aufweisen, oder auch unterschiedliche Mutationen im Cathepsin-C-Gen, selten durch Neumutationen. Die Eltern des Kindes als Träger eines einzelnen defekten Allels zeigen typischerweise keine Symptome des PLS. Trotzdem können sie aufgrund der hohen Prävalenz von einer allgemeinen Parodontitis betroffen sein. Die genetische Diagnose stützt sich auf die klinische Verdachtsdiagnose und wird durch den Nachweis pathogener Mutationen im Cathensin-C-Gen gesichert. Die Eltern als Überträger der Mutationen sollen in der Regel in die genetische Analyse mit einbezogen werden.
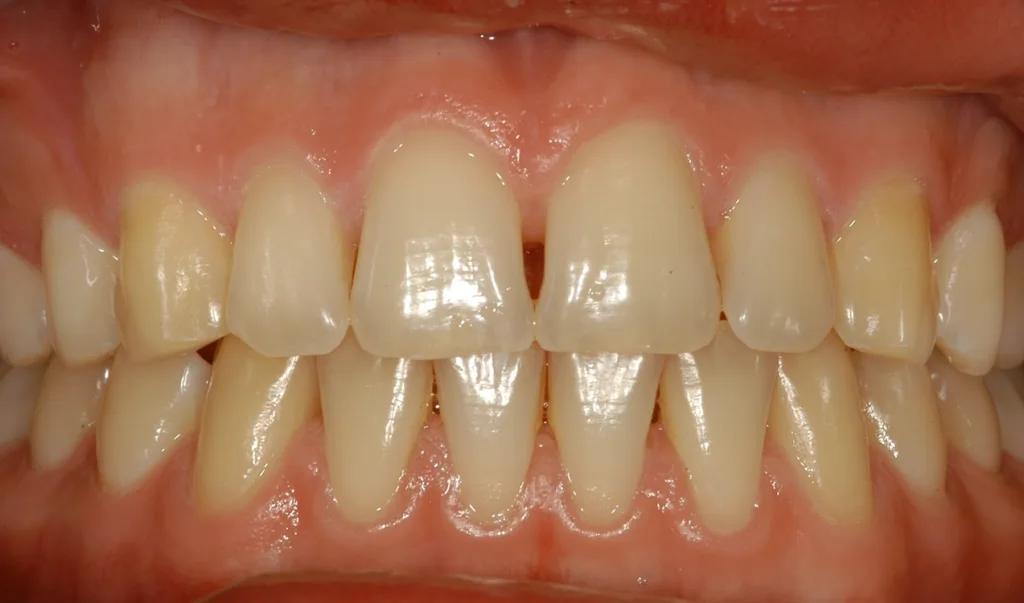
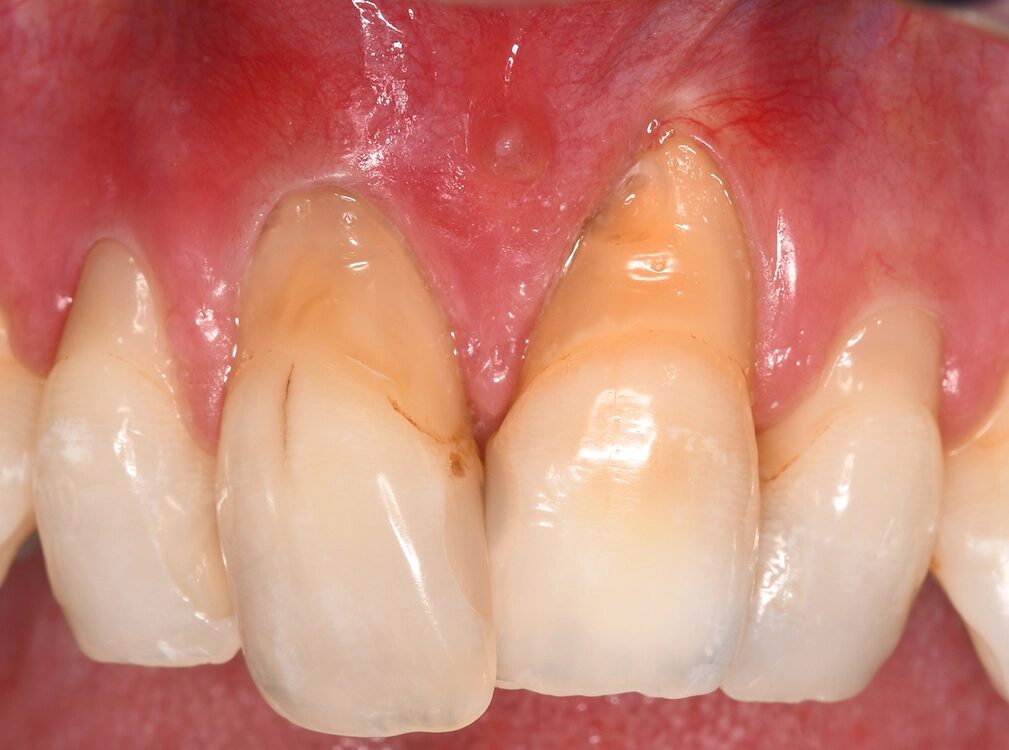
Die Ehlers-Danlos-Syndrome sind eine heterogene Gruppe von 13 unterschiedlichen Bindegewebserkrankungen, die alle durch Gelenkshypermobilitäten und überdehnbare und fragile Haut charakterisiert sind und je nach Typ mit unterschiedlichen weiteren Symptomen assoziiert sind [9]. Das parodontale Ehlers-Danlos-Syndrom (pEDS) ist das einzige der Ehlers-Danlos-Syndrome, das sich mit einer schweren Parodontitis im jugendlichen Alter, teilweise auch schon im Milchgebiss, manifestiert, da die Mutationen primär Gene der unspezifischen Immunantwort betreffen und erst in weiterer Folge die Bindegewebsschwäche verursachen [8] (Abb. 5, Abb. 6).
Die klinische Diagnose basiert auf der Trias der rasch progredienten Parodontitis im Teenageralter, dem kompletten Fehlen der befestigten Gingiva und der auffallenden Neigung zur Bildung von Hämatomen, die in zirka 80% der Betroffenen zu persistierenden Hämosiderin-Einlagerungen an den Schienbeinen führt. Die Parodontitis manifestiert sich teilweise schon im Milchgebiss, teilweise erst während der Pubertät und führt unbehandelt in wenigen Jahren zur Zahnlosigkeit. Das pEDS wird autosomal-dominant vererbt, sodass mindestens ein Elternteil ebenso an pEDS erkrankt ist; sehr selten kann es sich um eine Neumutation handeln. Die genetische Diagnose stützt sich auf die klinische Verdachtsdiagnose und wird durch den Nachweis pathogener Mutationen in den Komplement-1-Genen des C1S oder C1R gesichert.
Die Plasminogendefizienz ist eine seltene, autosomal-rezessiv vererbte Erkrankung, bei der der Körper zu wenig oder funktionsgestörtes Plasminogen produziert. Plasminogen ist ein Vorläuferenzym des Plasmins, das für den Abbau von Fibrin und anderen extrazellulären Proteinen entscheidend ist. Bei betroffenen Kindern führt der Mangel an funktionsfähigem Plasmin zu einer Ansammlung fibrinähnlicher Ablagerungen in Schleimhäuten, Augen, Atemwegen und gelegentlich der Haut. Typische orale Manifestationen sind gelblich-weiße Fibrinablagerungen auf der Mundschleimhaut, die mit lokalisierter parodontaler Destruktion einhergehen und diese maßgeblich bedingen [10]. Die Diagnose erfolgt durch den Nachweis reduzierter Plasminogenaktivität und genetischer Mutationen im PLG-Gen. Die Eltern als Überträger der Mutationen sollen in die genetische Analyse mit einbezogen werden.
Die Hypophosphatasie ist eine genetisch bedingte Stoffwechselerkrankung, bei der die Aktivität der alkalischen Phosphatase vermindert ist. Dadurch ist die Mineralisation von Knochen und Zähnen – besonders auch des Zements – gestört. Typische Zeichen sind Knochenverformungen, Frakturen, Muskelschwäche und ein erhöhtes Parodontitisrisiko, wobei die Prävalenz und die Schwere der Parodontitis besonders bei Patientinnen und Patienten mit zwei betroffenen Allelen deutlich höher ist und bereits ab den frühen 20ern auftreten kann [16]. Die Erkrankung hat unterschiedlich schwere Verlaufsformen – von schweren Formen im Säuglingsalter bis zu milden Varianten im Erwachsenenalter. Die Odontohypophosphatasie betrifft ausschließlich die Zähne, weshalb sie von Zahnärzten und Zahnärztinnen diagnostiziert werden muss. Typisch ist der frühe Verlust einzelner Milchzähne mit intakten Wurzeln, wobei die Prävalenz und das Alter bei Manifestation der Parodontitis in diesem Subtyp nicht abschließend geklärt sind.
Bei der zyklischen Neutropenie kommt es zu wiederkehrenden Abfällen der neutrophilen Granulozyten; typischerweise etwa alle 21 Tage. In diesen Phasen besteht eine erhöhte Infektanfälligkeit mit Symptomen wie Fieberschübe, Pharyngitis, Otitis media, Lymphadenitis sowie aphthoiden Läsionen der Mundschleimhaut. Zwischen den Zyklen ist das Blutbild meist normal, weshalb die systemische Diagnose durch Kinderärztinnen und -ärzte unter Umständen verzögert gestellt wird. Die Erkrankung wird überwiegend autosomal-dominant vererbt, weshalb häufig ein Elternteil betroffen ist, wobei die klinische Ausprägung variabel sein kann. Die Behandlung erfolgt häufig mit G-CSF, wodurch die Symptome deutlich reduziert werden können.
Parodontale Therapie im Kindes- oder Jugendalter
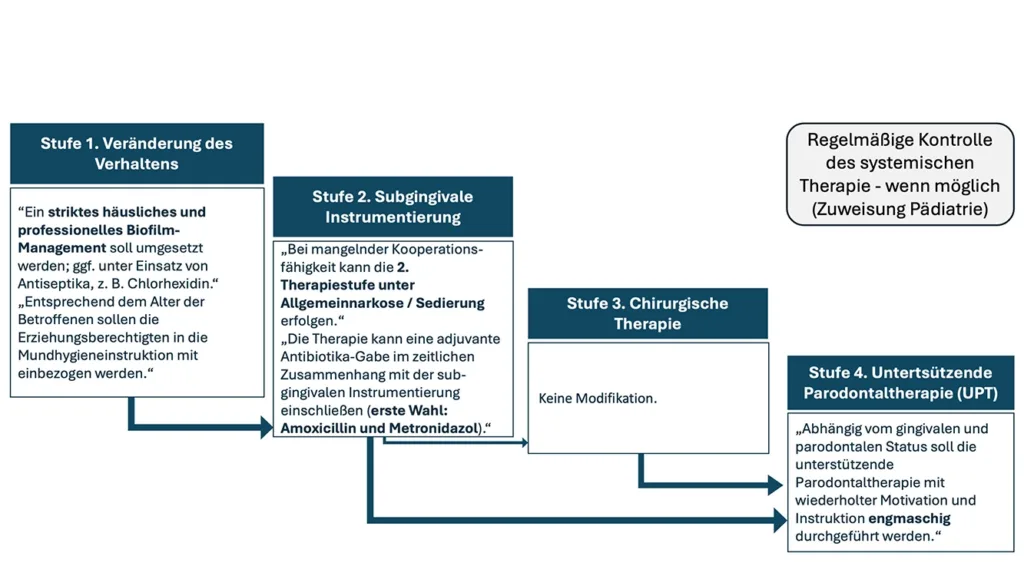
Prinzipiell unterscheidet sich die Therapie der Parodontitiden, die Teil einer seltenen Syndromerkrankung sind, nicht von der Therapie der Parodontitis im Allgemeinen, sodass die S3-Leitlinie „Die Behandlung von Parodontitis Stadium I bis III“ mit einigen Modifikationen angewandt werden kann [1] (Abb. 7). In der ersten Therapiestufe müssen so früh wie möglich speziell bei den Eltern das Bewusstsein und die Kompetenz für ein striktes Biofilmmanagement geschaffen werden. Da der Großteil der seltenen Erkrankungen, die sich mit einer Parodontitis manifestieren, immunologische Kompromittierungen darstellen, ist auch hier der dentale Biofilm der Auslöser der defizienten Immunantwort. Die Kinder sollen daher spielerisch, aber konsequent in die häusliche Mundhygiene eingeführt werden, wobei die Hauptverantwortung für eine regelmäßige und verlässliche Durchführung in jungen Jahren bei den Eltern liegt. Falls eine systemische Therapie der Grunderkrankung möglich ist, muss diese regelmäßig durch Pädiater und Pädiaterinnen kontrolliert und ggf. angepasst werden. Zahnärzte und Zahnärztinnen sollen vor allem bei einer Verschlechterung der oralen Befunde an eine möglicherweise notwendige Adaptation der systemischen Therapie denken. Alkoholfreie Chlorhexidinspülungen dürfen zeitlich begrenzt zur Anwendung kommen, wenn das Kind sicher ausspucken kann. Alternativ kann ein Chlorhexidinspray verwendet werden.
 Ines Kapferer-Seebacher
Ines Kapferer-SeebacherIn der zweiten Therapiestufe kann aufgrund der noch fehlenden Adhärenz für längere zahnmedizinische Behandlungen die subgingivale Instrumentierung unter Allgemeinanästhesie durchgeführt werden. Eine adjuvante systemische Antibiotikatherapie wird in diesem Zusammenhang häufig eingesetzt, typischerweise in Form einer Kombination aus Metronidazol und Amoxicillin in gewichtsadaptierter Dosierung. Insbesondere beim PLS scheint die Eradikation des Aggregatibacter actinomycetemcomitans eine Bedeutung zu haben. Auch wenn dieser Zusammenhang aufgrund der Seltenheit des Syndroms nicht abschließend geklärt ist, kann eine mikrobiologische Analyse vor und nach der Antibiose wertvolle Hinweise liefern.
Einzelne Fallberichte zeigten [11,14], dass erst wiederholte subgingivale Instrumentierungen in Kombination mit einer systemischen Antibiose zur Elimination von A. actinomycetemcomitans führten und in der Folge die parodontale Destruktion zum Stillstand kam. Darüber wurde in einzelnen Fällen beschrieben [2], dass beim PLS auch die Komplettextraktion des Milchgebisses mit anschließender zahnloser Phase bis zum Durchbruch der bleibenden Zähne erfolgreich sein kann, vermutlich infolge einer effektiven Eradikation des A. actinomycetemcomitans. Es ist jedoch anzumerken, dass die verfügbare Evidenz hierzu sehr begrenzt ist und ausschließlich das PLS betrifft. Für andere Syndrome mit früh einsetzender Parodontitis liegen derzeit keine Daten zu spezifischen mikrobiologischen Zusammenhängen vor. Eine adjuvante systemische Antibiotikatherapie kann dennoch im Einzelfall indiziert sein und sollte individuell unter Abwägung von Nutzen und Risiken entschieden und mit den Pädiaterinnen und Pädiatern abgestimmt werden.
Die dritte Therapiestufe wird in den bisher publizierten Fallberichten häufig vernachlässigt, sollte aber nach Meinung der Autoren und Autorinnen dieses Artikels konsequent durchgeführt werden. Diese Phase der Parodontaltherapie zielt bekanntlich auf die Behandlung der Bereiche der Dentition ab, welche nicht adäquat auf die zweite Therapiestufe reagiert haben, also tiefe parodontale Taschen ≥6 mm. Im Milchgebiss kann eine Extraktion der betroffenen Zähne in Erwägung gezogen werden, wiederholte subgingivale Instrumentierung einzelner Zähne mit oder ohne adjuvante Therapien können nun eventuell auch in Lokalanästhesie durchgeführt werden. In der medizinischen Fachliteratur werden parodontalchirurgische Maßnahmen auch schon bei Kindern – teilweise unter Allgemeinanästhesie – beschrieben [5]. Eine Nutzen-Risiko-Abwägung ist in enger Absprache mit den Betroffenen und den Eltern zu treffen.
Der vierten Therapiestufe kommt aufgrund des lebenslang erforderlichen, strikt durchgeführten Biofilmmanagements eine zentrale Bedeutung für den langfristigen Zahnerhalt der Betroffenen zu. Abhängig von der Kompetenz und Konsequenz der Eltern sowie des Kindes ist das Intervall der unterstützenden Parodontaltherapie individuell festzulegen und kann auch engmaschige, monatliche Termine erforderlich machen. Erfahrungswerte zeigen, dass insbesondere die transitorische Entwicklungsphase der Adoleszenz eine kritische Phase darstellt: In diesem Alter streben die Betroffenen verstärkt nach Eigenverantwortung, ohne die medizinischen Konsequenzen einer unzureichenden häuslichen Mundhygiene bereits mit der erforderlichen Tragweite zu erfassen. Gleichzeitig treten in dieser Lebensphase zusätzliche gesundheitsrelevante Verhaltensweisen auf, die das parodontale Risiko weiter erhöhen. Auch wenn die Ausgangsdiagnose zunächst aussichtslos erscheinen mag, zeigen gut dokumentierte Fallberichte [15], dass der Zahnerhalt bis ins Erwachsenenalter möglich ist. Entscheidend hierfür sind die Adhärenz der Betroffenen sowie die konsequente Einbindung und Unterstützung durch deren Betreuungspersonen. Vor diesem Hintergrund kommt der motivierenden Gesprächsführung, der umfassenden Aufklärung und der strukturierten Instruktion in eine effiziente häusliche Mundhygiene eine zentrale Bedeutung zu. Gleichzeitig besteht für Behandlerinnen und Behandler kein Anlass zur therapeutischen Zurückhaltung, da sich das zahnärztliche Vorgehen grundsätzlich nicht von etablierten parodontalen Behandlungskonzepten unterscheidet und vielmehr eine strukturierte, konsequente Betreuung erfordert.
Fazit
Eine Parodontitis im Kindes- oder Jugendalter ist stets als Warnsignal zu verstehen und sollte differenzialdiagnostisch an das Vorliegen einer seltenen syndromalen Erkrankung denken lassen. Auch wenn die Prognose bei syndromassoziierten Parodontitiden initial häufig ungünstig erscheint, zeigen gut dokumentierte Fallberichte, dass durch ein frühzeitiges, konsequent durchgeführtes und individuell angepasstes Therapiekonzept ein langfristiger Zahnerhalt bis ins Erwachsenenalter möglich ist. Entscheidend hierfür sind eine hohe Adhärenz der Betroffenen, die enge Einbindung und Schulung der Betreuungspersonen sowie eine lebenslange unterstützende Parodontaltherapie mit strikt durchgeführtem Biofilmmanagement. Neben der mechanischen Infektionskontrolle sind bei ausgewählten Syndromen adjuvante systemische Therapien, einschließlich Antibiotikagabe, sowie eine interdisziplinäre Zusammenarbeit mit Pädiatrie, Humangenetik und weiteren Fachdisziplinen essenziell.
Acknowledgement: Der Artikel basiert auf Inhalten von Gesprächen und Diskussionen mit den Autorinnen und Autoren der AWMF-S3-Leitlinie zur Versorgung seltener Erkrankungen in der Zahn-, Mund- und Kieferheilkunde.
 Entdecke CME Artikel
Entdecke CME Artikel  Entdecke Artikel mit Download
Entdecke Artikel mit Download 





 Mit Google einloggen
Mit Google einloggen
 Mit Facebook einloggen
Mit Facebook einloggen
Keine Kommentare.